Este análisis profundiza en la realidad actual del mercado minorista de medicamentos veterinarios en Rusia y la región de la Unión Económica Euroasiática (EAEU). A diferencia de los flujos de importación general, el sector minorista presenta una dinámica de consumo interna muy agresiva, pero atrapada en un complejo entramado regulatorio donde la armonización legislativa es todavía una meta lejana.
Como especialistas en RuGMP, analizamos por qué este escenario representa un desafío crítico para el fabricante europeo y dónde nuestra intervención técnica es determinante para evitar el rechazo de registros.
El Mercado Minorista Veterinario en Rusia (2025): Radiografía de una Fragmentación Regulatoria
El sector minorista veterinario en Rusia ha cerrado 2025 con cifras de consumo récord. Según el último informe de RNC Pharma, el mercado minorista (total sell-out) alcanzó los 49.200 millones de rublos (~518 M€), lo que representa un crecimiento del 17,7% en términos monetarios. Es fundamental subrayar que estas cifras corresponden estrictamente a la venta minorista; no estamos analizando importaciones brutas, sino el comportamiento del producto en el punto de venta final.
1. Dinámica del Mercado Minorista y Consumo
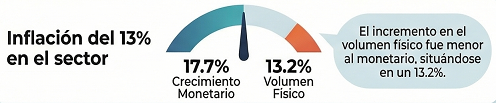
El crecimiento del mercado minorista se apoya en una inflación sectorial del 13% y un desplazamiento hacia productos de mayor costo.
- Premiumización: La cuota de medicamentos con un precio superior a los 1.000 rublos (~10 €) por unidad mínima de dosificación (MED) alcanzó el 24,9% del mercado minorista en valor.

- Crecimiento en Volumen: El mercado movilizó 276,8 millones de unidades (+13,2%), impulsado principalmente por el canal online, que ya representa el 27,9% de las ventas minoristas monetarias.
- Aliados Estratégicos: Mientras las ventas minoristas de productos de origen europeo caen drásticamente, Bielorrusia, aliado estratégico de Rusia y miembro pleno de la EAEU, ha disparado sus ventas en el mercado ruso un 54% respecto al año anterior.
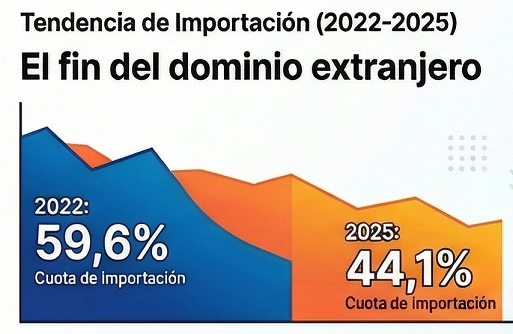
2. El Laberinto del Registro: Legislación Confusa y No Alineada
Para el fabricante europeo, el mayor obstáculo no es la demanda, sino una legislación que todavía se percibe confusa y con procesos no alineados. A pesar de los esfuerzos por crear un mercado común de medicamentos en la Unión Económica Euroasiática (EAEU), la realidad técnica actual es de fragmentación:
- Certificaciones Nacionales Vigentes: Por el momento, los registros en cada país miembro exigen el certificado GMP nacional. Esto implica que, para registrar un producto en Rusia, se exige el certificado GMP ruso emitido por las autoridades locales; para Bielorrusia, su certificado nacional correspondiente.
- Inspecciones Activas: Actualmente, las inspecciones a fabricantes de medicamentos veterinarios son realizadas de forma separada por los organismos nacionales. En Rusia, esta labor recae en el Centro estatal ruso para la calidad y estandarización de los medicamentos veterinarios y piensos (VGNKI), mientras que en Bielorrusia es gestionada por el Centro estatal veterinario de Belarús (BGVC).
- La Brecha con el Uso Humano: Es vital entender que la admisión y el reconocimiento de certificados GMP para uso veterinario no sigue el mismo ritmo que para medicamentos de uso humano. El sector veterinario tiene todavía mucho camino por delante para lograr la reciprocidad total que ya se vislumbra en el sector de salud humana.

3. Estadísticas de Denegación para el Fabricante Extranjero
El rigor de las autoridades nacionales, como el VGNKI de Rusia, ha creado un «embudo» que afecta desproporcionadamente a los productos internacionales, informa el portal ruso de industria farmacéutica Pharmprom.

- Ratio de Registro: En 2025, se registraron 4,5 veces más fármacos veterinarios nacionales que extranjeros (88 frente a 19).
- Causas de Rechazo: De las 37 denegaciones de registro documentadas, 22 correspondieron a fármacos extranjeros debido a la incapacidad de confirmar la seguridad de los datos según los estándares rusos.
- Costes Elevados: La tasa estatal por el peritaje de un nuevo medicamento veterinario asciende a 461.000 rublos (~4900 €). Queremos destacar que el coste de la inspección para obtener el certificado GMP no está incluido en esta tasa.
4. ¿Cómo actúa RuGMP en este entorno?
Dada la confusión legislativa y la exigencia de certificados nacionales dobles o triples, la proactividad es la única forma de evitar el fracaso del registro. En RuGMP, proporcionamos el soporte técnico necesario para navegar esta fase de transición:
- Aclaraciones sobre el Proceso: Ayudamos a los fabricantes a entender los pasos específicos requeridos por el VGNKI (Rusia) y el BGVC (Bielorrusia), asegurando que el dossier cumpla con las normas de cada jurisdicción.
- Preparación para Certificación GMP: Preparamos a los laboratorios europeos para las inspecciones nacionales, centrándonos en las diferencias de criterios que todavía existen entre las agencias.
- Traducción e Interpretación Farmacéutica: Durante las inspecciones y auditorías GMP, proporcionamos interpretación técnica en ruso, español e inglés, garantizando que la comunicación científica con los inspectores sea exacta y libre de errores interpretativos que podrían derivar en deficiencias críticas.
Conclusión
Se espera que, en un futuro cercano, los certificados de la EAEU tengan la misma validez en todo el territorio de la Unión. Sin embargo, mientras ese momento llega, el fabricante europeo debe gestionar múltiples normativas nacionales simultáneamente. El éxito en el mercado minorista de la región depende de una defensa técnica impecable y de una comprensión profunda de una legislación que aún está en proceso de maduración.






