Con la implementación de la Decisión n.º 60, el proceso de registro de medicamentos en la EAEU integra un sistema de inspección GLP que no solo verifica documentos, sino que evalúa la integridad científica del dato desde su origen. Para los laboratorios y Sponsors europeos, lo más relevante es el enfoque basado en riesgos que determina cómo y qué será inspeccionado.
¿Qué cambia realmente para el sector?
El cambio fundamental radica en la transición de una revisión administrativa a una supervisión técnica activa del cumplimiento de las normas de GLP, Good Laboratory Practices.
- Formatos de Inspección: La autoridad ahora puede optar por inspecciones presenciales, documentales o mediante medios remotos (audio y video) en casos de fuerza mayor o emergencias sanitarias.
- Selección por Riesgo: El formato de la inspección se decide según la complejidad del producto y el historial de cumplimiento del centro. Los laboratorios sin inspecciones previas de la EAEU suelen clasificarse como de Riesgo Moderado/Alto.
- Alcance al Sponsor: La potestad inspectora se extiende más allá del laboratorio de ensayo, alcanzando las instalaciones del Sponsor (promotor) y cualquier organización que participe en el estudio.
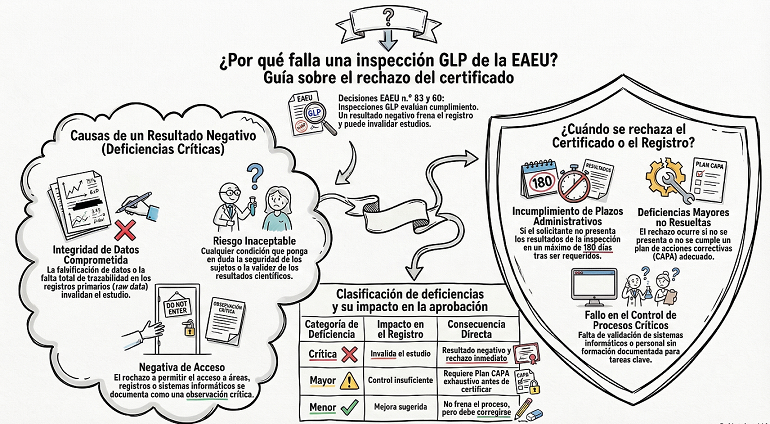
Clasificación de Deficiencias y su Impacto
Durante la inspección, las no conformidades se categorizan según su gravedad, determinando directamente el futuro del registro:
1. Deficiencias Críticas
Son aquellas que representan un riesgo inaceptable para la validez de los datos o la seguridad de los sujetos.
- Impacto: Invalidan el estudio preclínico.
- Ejemplos: Falsificación de datos, falta total de trazabilidad en el raw data, o condiciones de laboratorio que comprometen totalmente la integridad del espécimen investigado.
- Consecuencia: Resultado de inspección negativo.
2. Deficiencias Mayores
Son desviaciones significativas de las normas de Buenas Prácticas de Laboratorio (GLP).
- Impacto: No invalidan el estudio de inmediato, pero indican que el Sponsor o el laboratorio no tienen un control suficiente sobre los procesos críticos.
- Ejemplos: Falta de validación de sistemas informáticos críticos, desviaciones no documentadas en el protocolo o personal sin la formación específica documentada para tareas clave.
- Consecuencia: Requieren un plan de acciones correctivas y preventivas (CAPA) exhaustivo antes de recibir el certificado de conformidad.
3. Deficiencias Menores
Son desviaciones que no afectan a la validez de los datos ni a la seguridad.
- Impacto: Son observaciones de mejora o errores aislados.
- Ejemplos: Errores tipográficos menores en registros no críticos o falta de orden en archivos que no afecta a la recuperación de la información.
- Consecuencia: Se deben corregir, pero no suelen frenar el proceso de registro.
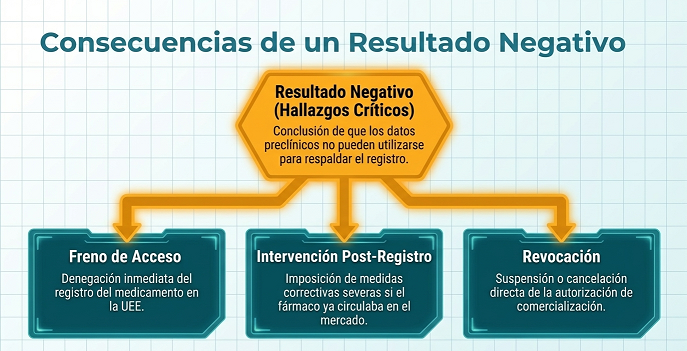
El Impacto en las Empresas Europeas
Para las compañías que operan desde la UE, la Decisión n.º 60 elimina la barrera de la distancia. Si una empresa se niega a facilitar el acceso a los inspectores (ya sea físico o remoto), dicho rechazo se documenta y puede invalidar completamente el dossier de registro.
Además, los plazos son estrictos: tras recibir el informe, el Sponsor dispone de solo 20 días hábiles para presentar su respuesta y el plan CAPA correspondiente.
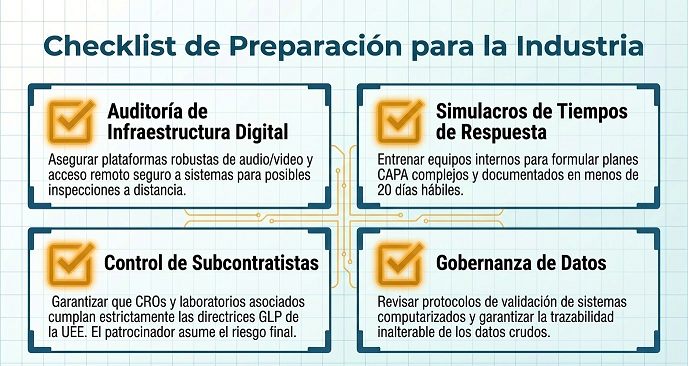
El Apoyo Técnico de RuGMP
En RuGMP, entendemos que la precisión técnica es la única defensa ante una inspección internacional. Ofrecemos soporte especializado en dos áreas críticas:
Intérpretes Científicos: Proporcionamos intérpretes expertos en las normas de GLP, Good Laboratory Practices que aseguran que la comunicación técnica entre los científicos europeos y los inspectores sea exacta y libre de errores interpretativos.
Consultoría para CAPA y Documentación: Asesoramos en la elaboración de planes de acciones correctivas que cumplan con los estándares de evaluación de la EAEU para evitar el rechazo del registro.
Conclusión
La Decisión n.º 60 eleva el nivel de exigencia para el acceso a los mercados de la EAEU. La clave para los laboratorios en la UE será la transparencia en sus acuerdos de calidad y la robustez de sus sistemas de gestión de datos. Una preparación adecuada garantiza que estas inspecciones se conviertan en una ventaja competitiva para operar en la región.