El 10 de marzo de 2026 entran en vigor las nuevas normas de la Unión Económica Euroasiática (EAEU) para Ensayos Clínicos, según lo establecido en la Decisión n.º 63. Este cambio busca unificar los criterios de cumplimiento y simplificar el proceso de registro dentro de la región, alineándose más estrechamente con los estándares internacionales de la ICH GCP.
1. Cambios operativos inmediatos
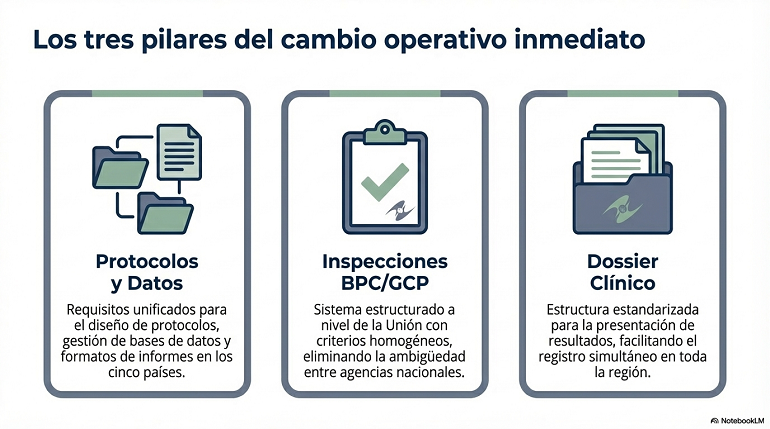
La transición hacia un reglamento supranacional simplifica la burocracia a largo plazo, pero exige una actualización técnica inmediata en la gestión de los estudios:
- Protocolos y datos unificados: Los cinco estados miembros (Armenia, Bielorrusia, Kazajistán, Kirguistán y Rusia) compartirán los mismos requisitos para el diseño de protocolos, gestión de bases de datos y formatos de informes.
- Inspecciones de BPC (GCP): Se establece un sistema de inspecciones de la Unión Euroasiática más estructurado. Las autoridades podrán auditar centros y procesos con criterios homogéneos, reduciendo la ambigüedad que existía entre agencias nacionales.
- Dossier clínico: La estructura para la presentación de resultados de ensayos clínicos se estandariza, facilitando el registro simultáneo en toda la región de la EAEU.
2. Impacto práctico para laboratorios europeos
Para las compañías españolas y europeas que operan o planean entrar en este mercado, las nuevas normas de ensayos clínicos definen reglas de juego más claras en cuanto al uso de datos generados en el extranjero:
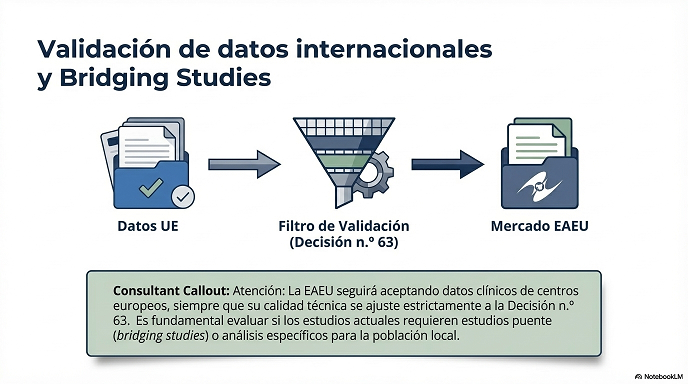
Validación de datos internacionales: La EAEU seguirá aceptando datos clínicos de centros europeos, siempre que la calidad técnica se ajuste estrictamente a la Decisión n.º 63. Es fundamental evaluar si los estudios actuales requieren estudios puente (bridging studies) o análisis específicos para esta población.

Auditorías transfronterizas: Las agencias de la EAEU tienen ahora el marco legal para realizar inspecciones de cumplimiento de GCP en centros de investigación situados en la Unión Europea si estos aportan datos críticos para un registro en su región.
- Farmacovigilancia: Los procesos de reporte de seguridad y los Informes Periódicos de Actualización de Seguridad (PSUR) deben integrarse bajo la nueva estructura técnica de la Unión.
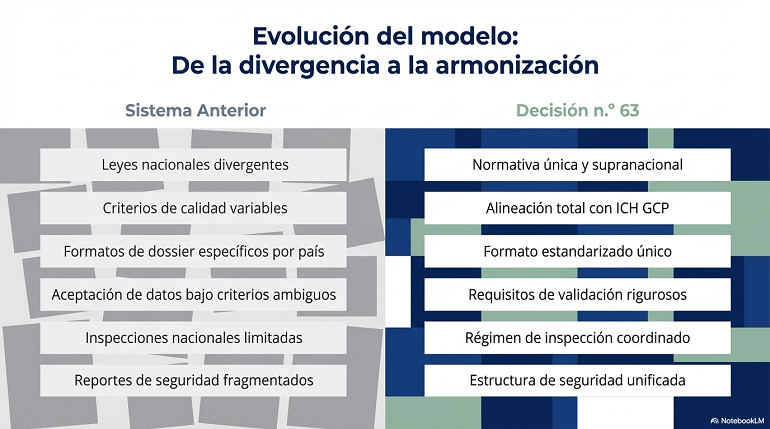
3. Consideraciones técnicas y de transición
El principal reto para los departamentos de Regulatory Affairs y Clinical Operations es asegurar que los estudios clínicos en curso no queden obsoletos.
Conclusión técnica: Una planificación temprana permitirá que el paquete de datos clínicos sea válido tanto para la EMA como para la EAEU, evitando duplicidades y optimizando la inversión en I+D. La clave reside en realizar auditorías de cumplimiento preventivas antes de la implementación total en marzo de 2026.






